近段時間,來自美國紐約阿爾伯特-愛因斯坦醫學院腫瘤學系的Yun-Ruei Kao教授及團隊開發了允許瞬時鐵生物利用度限制的模型,并將單分子 RNA 定量、代謝組學和單細胞轉錄組分析與功能研究相結合,旨在研究鐵限制的功能和分子后果。
結果顯示,HSPCs限制其LIP,并在穩定狀態下表現出持續的有限鐵反應,這種反應在有絲分裂期間和實驗性急性鐵限制時會增強,揭示了有絲分裂期間的新陳代謝需求可有效觸發 HSPCs 中鐵平衡途徑的激活。賴氨酸乙酰轉移酶 Tip60/KAT5 可能通過乙酰化和激活 Lipin1,在 HSPC 脂質合成中發揮了核心作用。該實驗數據顯示,LIP限制作為一種獨特的分子中繼,在再生壓力下許可特定的代謝途徑--尤其是已知可擴大造血干細胞池的FAO。該團隊還證明細胞質鐵負荷通過損害FA代謝和依賴Tip60的基因調控,支撐干細胞衰老。
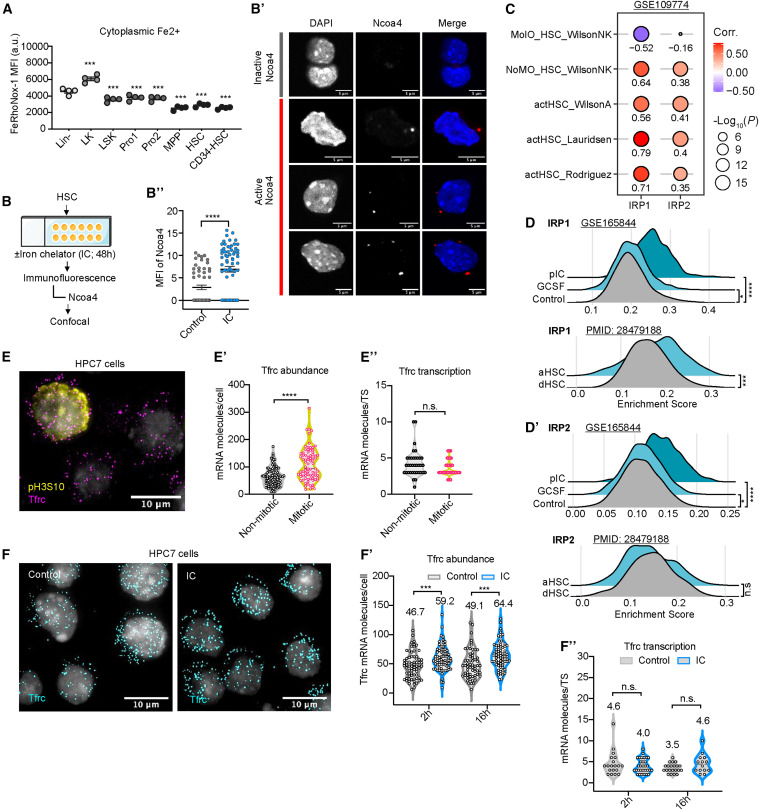
LIP 限制會激活造血干細胞的有限鐵反應
總之,鐵限制反應的激活引發了協調的代謝和表觀遺傳事件,建立了干性強化基因調控,該團隊證明了衰老相關的細胞質鐵負荷會可逆地削弱鐵依賴的細胞命運控制,從而解釋了針對功能失調的衰老干細胞的干預策略。
來源:網絡

相關閱讀:
助力生物醫藥高質發展:細胞基因治療實驗室技術設計要點 CEIDI西遞
生物醫藥工程建設:分子生物與蛋白純化實驗室設計
生物安全實驗室裝修要求 CEIDI西遞